
ESTADOS DE LA MATERIA
- Sólidos:
- Liquido
- Gaseoso
Dadas las condiciones existentes en la superficie terrestre, sólo algunas sustancias pueden hallarse de modo natural en los tres estados, tal es el caso del agua.
La mayoría de sustancias se presentan en un estado concreto. Así, los metales o las sustancias que constituyen los minerales se encuentran en estado sólido y el oxígeno o el CO2 en estado gaseoso.
- Los Sólidos:Tienen formas y volumen constante. Se caracterizan por la rigidez y regularidad de su estructura.
- Los Líquidos: No tienen forma fija pero sí volumen. La variabilidad de forma y el presentar unas propiedades muy específicas son características de los líquidos.
- Los Gases: No tienen forma ni volumen fijos. En ellos es muy característica la gran variación de volumen que experimentan al cambiar las condiciones de temperatura y presión.
Sólido:
Los cuerpos sólidos, son aquellos que mantienen forma y volumen constantes gracias a la gran cohesión de sus moléculas.
 Entre las propiedades de los sólidos, se destacan la elasticidad (un sólido puede recuperar su forma original cuando es deformado), la dureza (no puede ser rayado por otro cuerpo más blanco) y la fragilidad (los sólidos pueden romperse en muchos pedazos ya que son quebradizos)
Entre las propiedades de los sólidos, se destacan la elasticidad (un sólido puede recuperar su forma original cuando es deformado), la dureza (no puede ser rayado por otro cuerpo más blanco) y la fragilidad (los sólidos pueden romperse en muchos pedazos ya que son quebradizos)
Los líquidos, al igual que los sólidos, tienen volumen constante. En los líquidos las partículas están unidas por unas fuerzas de atracción menores que en los sólidos, por esta razón las partículas de un líquido pueden trasladarse con libertad. El número de partículas por unidad de volumen es muy alto, por ello son muy frecuentes las colisiones y fricciones entre ellas.
 Así se explica que los líquidos no tengan forma fija y adopten la forma del recipiente que los contiene. También se explican propiedades como la fluidez o la viscosidad.
Así se explica que los líquidos no tengan forma fija y adopten la forma del recipiente que los contiene. También se explican propiedades como la fluidez o la viscosidad.En los líquidos el movimiento es desordenado, pero existen asociaciones de varias partículas que, como si fueran una, se mueven al unísono. Al aumentar la temperatura aumenta la movilidad de las partículas (su energía).

GAS:
Los gases, igual que los líquidos, no tienen forma fija pero, a diferencia de éstos, su volumen tampoco es fijo. También son fluidos, como los líquidos.
En los gases, las fuerzas que mantienen unidas las partículas son muy pequeñas. En un gas el número de partículas por unidad de volumen es también muy pequeño.

Las partículas se mueven de forma desordenada, con choques entre ellas y con las paredes del recipiente que los contiene.
Esto explica las propiedades de expansibilidad y compresibilidad que presentan los gases: sus partículas se mueven libremente, de modo que ocupan todo el espacio disponible. La compresibilidad tiene un límite, si se reduce mucho el volumen en que se encuentra confinado un gas éste pasará a estado líquido.

Al aumentar la temperatura las partículas se mueven más deprisa y chocan con más energía contra las paredes del recipiente, por lo que aumenta la presión.
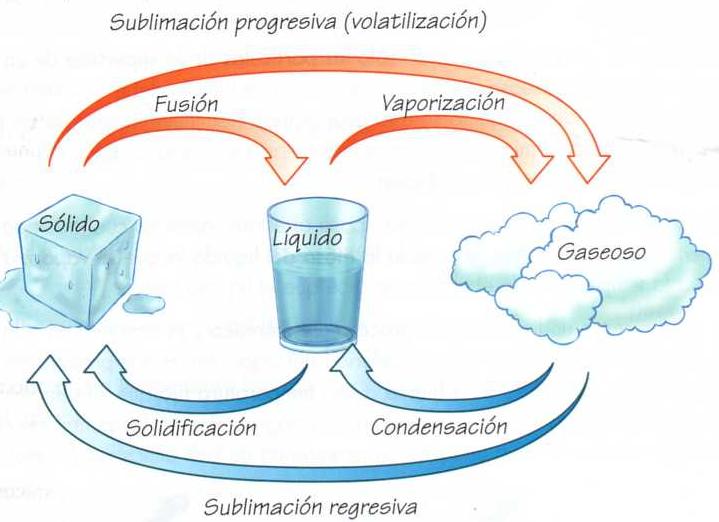
Cambio De Estados
Cuando un cuerpo, por acción del calor o del frío pasa de un estado a otro, decimos que ha cambiado de estado. En el caso del agua: cuando hace calor, el hielo se derrite y si calentamos agua líquida vemos que se evapora.
El resto de las sustancias también puede cambiar de estado si se modifican las condiciones en que se encuentran. Además de la temperatura, también la presión influye en el estado en que se encuentran las sustancias.
Si se calienta un sólido, llega un momento en que se transforma en líquido. Este proceso recibe el nombre de fusión. El punto de fusión es la temperatura que debe alcanzar una sustancia sólida para fundirse. Cada sustancia posee un punto de fusión característico.
Por ejemplo, el punto de fusión del agua pura es 0°C a la presión atmosférica normal.
Si calentamos un líquido, se transforma en gas.
Este proceso recibe el nombre de vaporización. Cuando la vaporización tiene lugar en toda la masa de líquido, formándose burbujas de vapor en su interior, se denomina ebullición.
También la temperatura de ebullición es característica de cada sustancia y se denomina punto de ebullición. El punto de ebullición del agua es 100°C a la presión atmosférica
normal.


No hay comentarios:
Publicar un comentario